トップメッセージ
Top message
トップ>JCRより皆さまへ>株主・投資家の皆さまへ>トップメッセージ


Q1当期(2023年4月1日から2024年3月31日まで)の業績の概要をお聞かせください。
A1売上高は428億71百万円(前期比24.8%増)となりました。
売上高につきましては、主力製品が好調に推移し、契約金収入やその他として計上される受託製造分の売上が増加した結果、前期比で増収となりました。
利益面につきましては、主力製品の売上増加に伴う販促費用の増加や、積極的な研究開発活動による研究開発費の増加があったものの、売上高の増収により、各利益は前期比で大幅な増益となりました。
Q2株主還元策についてお聞かせください。
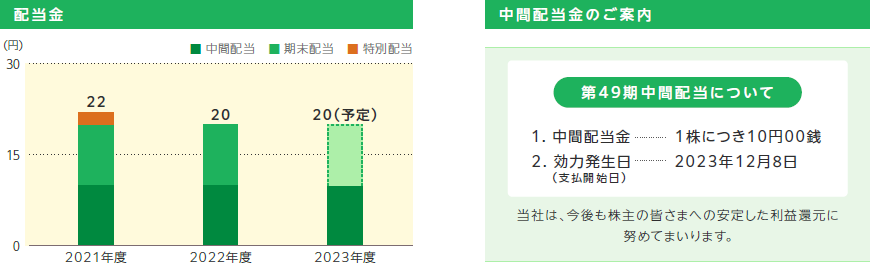
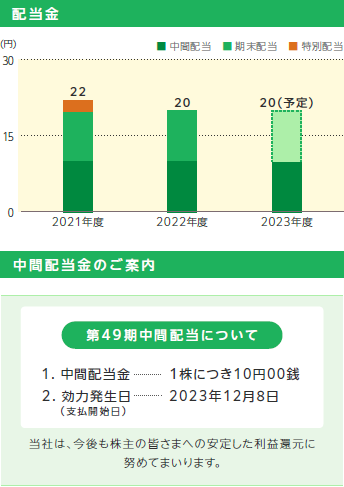
A2期末配当金は1株当たり10円00銭となります。
剰余金の配当等の決定に関しては、将来の利益の源泉となる新薬開発や経営体質強化のための内部留保を確保しつつ、業績およびキャッシュ・フローの状況などを勘案しながら継続的かつ安定的な配当を行うことを基本方針としております。当該方針のもと、2024年3月期の期末配当は、直近の配当予想のとおり1株当たり10円00銭とさせていただきます。内部留保資金につきましては、企業体質を強化し、持続的な収益向上と利益還元に寄与する原資として有効活用してまいります。
Q3JCRで開発中の新しい遺伝子治療技術について教えてください。
A3J-Brain Cargo®と遺伝子治療を融合した技術の開発を進めています。
当社は、1975年の創業当初から培ってきたバイオ医薬品の高度な技術力とノウハウを有しており、それらを基盤としてJ-Brain Cargo®(以下、JBC)という血液脳関門通過技術の実用化に世界で初めて成功しました。このJBCと遺伝子治療を融合した技術の開発を進めています。具体的には、①JBC融合タンパク質を発現するアデノ随伴ウイルス(AAV)による治療、②JBCを表面に修飾したAAVによる治療の2種類です。特に②に関しては、従来の遺伝子治療ではターゲットにすることが困難であった膜タンパク質にも適応可能であり、今後ライソゾーム病だけでなく、幅広い疾患の治療薬に応用されることを期待しています。

